
Актемра, раствор, 162 мг 0.9 мл ×4
для подкожного введения шприцы преднаполненные, Роше, Швейцария • Без рецепта
Караганда
Каталог
Действующее вещество: Тоцилизумаб

для подкожного введения шприцы преднаполненные, Роше, Швейцария • Без рецепта
Антинеопластические и иммуномодулирующие препараты. Иммуносупрессанты. Ингибиторы интерлейкина. Тоцилизумаб.
Код АТХ L04AC07
Препарат Актемра® в комбинации с метотрексатом (МТ) показан для лечения:
● тяжелого, активного и прогрессирующего ревматоидного артрита у взрослых пациентов, ранее не получавших лечение МТ
● РА средней или высокой степени активности у взрослых пациентов, с недостаточным клиническим ответом на предыдущую терапию болезнь-модифицирующими антиревматическими препаратами (БМАРП) или непереносимостью одного или более БМАРП или антагонистов фактора некроза опухоли (ФНО).
У данных пациентов препарат Актемра® может назначаться в качестве монотерапии в случае непереносимости МТ или если продолжение лечения МТ является нецелесообразным.
Согласно рентгенологическим данным было показано, что применение препарата Актемра® в комбинации с метотрексатом тормозит прогрессирования деструкции суставов и улучшает их функцию.
Препарат Актемра® показан для лечения пациентов в возрасте 1 года и старше с активным системным ювенильным идиопатическим артритом с неадекватным ответом на предшествующую терапию нестероидными противовоспалительными препаратами и системными кортикостероидами. Препарат Актемра® может назначаться в качестве монотерапии (в случае непереносимости МТ или нецелесообразности лечения МТ) или в комбинации с МТ.
Препарат Актемра® в комбинации с метотрексатом показан для лечения полиартикулярного ювенильного идиопатического артрита (положительный или отрицательный ревматоидный фактор и распространенный олигоартрит) у пациентов в возрасте 2 лет и старше с неадекватным ответом на предшествующую терапию МТ.
Препарат Актемра® может назначаться в качестве монотерапии в случае непереносимости МТ или если продолжение лечения МТ является нецелесообразным.
Препарат Актемра® показан для лечения гигантоклеточного артериита у взрослых пациентов.
− гиперчувствительность к активному веществу или к любому из вспомогательных веществ
− тяжелые инфекции в активной стадии.
Препарат Актемра® в лекарственной форме для подкожного введения не предназначен для внутривенного введения.
Препарат Актемра® в лекарственной форме для подкожного введения не предназначен для лечения детей с системным ювенильным идиопатическим артритом с массой тела менее 10 кг.
Инфекции
У пациентов, получавших иммунодепрессанты, в том числе препарат Актемра®, сообщалось о случаях развития серьезных инфекций, иногда с летальным исходом.
Туберкулез
Как и при назначении других биологических препаратов, перед началом терапии препаратом Актемра®, пациенты с РА, сЮИА или пЮИА, должны пройти обследование на латентную форму туберкулеза. Пациентам с латентным ТБ перед началом лечения препаратом Актемра следует провести стандартный курс антимикобактериальной терапии.
Реактивация вирусных инфекций
У пациентов с ревматоидным артритом, получавших терапию биологическими препаратами, сообщалось о случаях реактивации вирусной инфекции (например, вирусного гепатита В).
Осложнения дивертикулита
О случаях прободений дивертикула, как осложнений дивертикулита при применении препарата Актемра у пациентов с РА, сообщалось нечасто.
Реакции гиперчувствительности
На фоне применения препарата Актемра® сообщалось о случаях развития серьезных реакций гиперчувствительности, включая анафилаксию.
Активное заболевание печени и нарушение функции печени
Терапия препаратом Актемра®, особенно одновременно с метотрексатом, может быть ассоциирована с повышением активности «печеночных» трансаминаз, поэтому при назначении препарата пациентам с активным заболеванием печени или нарушением функции печени следует проявлять осторожность.
Гепатотоксичность
Во время лечения препаратом Актемра® сообщалось о транзиторном или интермиттирующем легком и умеренном повышении активности печеночных трансаминаз.
При применении препарата Актемра® наблюдались случаи лекарственно-индуцированного поражения печени, включая острую печеночную недостаточность, гепатит и желтуху.
Гематологические нарушения
При применении тоцилизумаба в комбинации с метотрексатом было отмечено снижение числа нейтрофилов и тромбоцитов. У пациентов, ранее получавших терапию антагонистами фактора некроза опухоли, возможен повышенный риск развития нейтропении.
Показатели липидного обмена
У пациентов, получавших лечение препаратом Актемра® наблюдалось повышение показателей липидного обмена, в том числе общего холестерина, липопротеинов низкой плотности, липопротеинов высокой плотности и триглицеридов.
Неврологические расстройства
В настоящее время о способности препарата Актемра® вызывать демиелинизирующие заболевания центральной нервной системы неизвестно.
Злокачественные новообразования
У пациентов с ревматоидным артритом повышен риск развития злокачественных новообразований. Иммуномодулирующие препараты могут повышать риск развития злокачественных новообразований.
Вакцинация
Не следует проводить иммунизацию живыми и живыми ослабленными вакцинами одновременно с терапией препаратом Актемра®, поскольку клиническая безопасность подобного сочетания не установлена.
Риск сердечно-сосудистых осложнений
У пациентов с ревматоидным артритом имеется повышенный риск развития сердечно-сосудистых заболеваний.
Комбинация с антагонистами фактора некроза опухоли (ФНО)
Опыт применения препарата Актемра® с антагонистами ФНО или другими биологическими препаратами для лечения ревматоидного артрита отсутствует.
Гигантоклеточный артериит
Не следует назначать препарат Актемра® в качестве монотерапии для лечения острых рецидивов, поскольку эффективность применения препарата в данном случае не установлена.
Системный ювенильный идиопатический артрит (сЮИА)
У пациентов с сЮИА возможен риск развития синдрома активации макрофагов, серьезного жизнеугрожающего состояния.
Одновременное однократное введение препарата Актемра® в дозе 10 мг/кг массы тела и метотрексата в дозе 10-25 мг один раз в неделю не оказывало клинически значимого влияния на экспозицию метотрексата.
Влияния метотрексата, нестероидных противовоспалительных препаратов или глюкокортикостероидов на клиренс препарата Актемра® у пациентов с ревматоидным артритом не установлено. У пациентов с гигантоклеточным артериитом кумулятивные дозы глюкокортикостероидов не оказывали влияния на экспозицию препарата Актемра®.
Экспрессия «печеночных» изоферментов системы CYP450 подавляется под действием цитокинов, таких как ИЛ-6, которые стимулируют хроническое воспаление. Таким образом, при проведении терапии средствами, ингибирующими действие цитокинов, например, препаратом Актемра®, экспрессия изоферментов CYP450 может быть нарушена.
ИЛ-6 вызывает снижение экспрессии изоферментов CYP1A2, CYP2C9, CYP2C19 и CYP3A4. Применение препарата Актемра® нормализует экспрессию этих изоферментов.
У пациентов с ревматоидным артритом концентрация симвастатина (субстрат СYP3A4) через 1 неделю после однократного введения тоцилизумаба снижается на 57%.
В начале или при завершении курса терапии тоцилизумабом следует тщательно наблюдать за пациентами, получающими лекарственные средства в индивидуально подобранных дозах, и которые метаболизируются посредством изоферментов CYP450 3A4, 1A2 или 2C9 (например, метилпреднизолон, дексаметазон (с возможностью развития синдрома отмены глюкокортикостероидов, предназначенных для приема внутрь), аторвастатин, блокаторы кальциевых каналов, теофиллин, варфарин, фенпрокумон, фенитоин, циклоспорин или бензодиазепины), поскольку для обеспечения терапевтического действия этих препаратов может потребоваться увеличение их дозы. Учитывая длительный период полувыведения тоцилизумаба, его действие на активность изоферментов CYP450 может сохраняться в течение нескольких недель после прекращения терапии.
Применение в педиатрии
Безопасность и эффективность препарата Актемра® в лекарственной форме для подкожного введения у новорожденных и детей младше 1 года не установлены. Данные отсутствуют.
Изменение дозы препарата возможно исключительно в случае стойкого изменения массы тела пациента с течением времени.
Пожилые пациенты
Коррекция дозы у пожилых пациентов в возрасте >65 лет не требуется.
Нарушение функции почек
Коррекция дозы у пациентов с нарушением функции почек легкой или умеренной степени тяжести не требуется. Применение препарата Актемра® у пациентов с тяжелой почечной недостаточностью не изучалось. У данных пациентов следует тщательно контролировать функцию почек.
Нарушение функции печени
Применение препарата Актемра® у пациентов с нарушением функции печени не изучалось.
Женщины с репродуктивным потенциалом
Женщины с репродуктивным потенциалом должны использовать эффективные средства контрацепции во время лечения и в течение 3 месяцев после окончания терапии.
Не следует применять препарат Актемра® во время беременности при отсутствии обоснованной клинической необходимости.
Неизвестно, выводится ли тоцилизумаб с грудным молоком у человека. При принятии решения о продолжении/прерывании кормления грудью или продолжении/отмене терапии препаратом Актемра® следует принимать во внимание пользу грудного вскармливания для ребенка и пользу терапии для матери.
Препарат Актемра® оказывает незначительное влияние на способность управлять транспортными средствами и потенциально опасными механизмами.
Режим дозирования
Ревматоидный артрит
Рекомендуемая доза препарата для подкожного введения составляет 162 мг один раз в неделю.
Гигантоклеточный артериит
Рекомендуемая доза препарата для подкожного введения составляет 162 мг один раз в неделю в комбинации с глюкокортикостероидами с постепенным снижением дозы последних.
Системный ювенильный идиопатический артрит
Рекомендуемая доза для пациентов старше 1 года с массой тела ≥30 кг составляет 162 мг 1 раз в неделю или 162 мг 1 раз в 2 недели подкожно для пациентов с массой тела менее 30 кг.
Минимальная масса тела пациентов при подкожном введении препарата Актемра® должна составлять 10 кг.
Полиартикулярный ювенильный идиопатический артрит
Рекомендуемая доза для пациентов старше 2 лет с массой тела ≥30 кг составляет 162 мг 1 раз в 2 недели или 162 мг 1 раз в 3 недели подкожно для пациентов с массой тела менее 30 кг.
Метод и путь введения
Препарат Актемра® предназначен для подкожного введения.
Пациенты могут самостоятельно вводить инъекцию препарата Актемра® только с разрешения врача после прохождения соответствующего обучения необходимой технике выполнения инъекций. Все содержимое (0.9 мл) шприц-тюбика следует ввести путем подкожной инъекции. Следует каждый раз менять рекомендуемые места инъекций (область живота, бедро и плечо), нельзя вводить препарат в родинки, шрамы, синяки или участки с нежной либо грубой кожей, покраснениями, уплотнениями или повреждениями.
Шприц-тюбик нельзя встряхивать.
Препарат Актемра поставляется в виде одноразового шприц-тюбика, оснащенного защитным устройством для иглы. После извлечения шприц-тюбика из холодильника, перед выполнением инъекции необходимо подождать 25-30 минут для того, чтобы раствор согрелся до комнатной температуры (18 °С – 25 °С). Шприц-тюбик не следует встряхивать. После снятия защитного колпачка с иглы, инъекцию необходимо выполнить в течение 5 минут; в противном случае раствор может высохнуть и заблокировать просвет иглы. В случае если шприц-тюбик не был использован в течение 5 минут после снятия колпачка, необходимо выбросить шприц в контейнер для утилизации острых инструментов, и вместо него следует использовать новый шприц-тюбик.
Если после введения иглы не удается опустить поршень шприца, необходимо выбросить шприц в контейнер для утилизации острых инструментов и подготовить новый шприц-тюбик.
Нельзя использовать шприц-тюбик в случае помутнения раствора или наличия в препарате посторонних видимых частиц, изменения цвета (раствор должен быть от бесцветного до светло-желтого цвета) или признаков повреждения любых частей шприц-тюбика.
Утилизация
Любое неиспользованное количество лекарственного препарата следует утилизировать.
Длительность лечения
Гигантоклеточный артериит
Ввиду хронического характера течения гигантоклеточного артериита продолжение терапии после 52 недели должно проводиться с учетом активности заболевания по усмотрению врача, а также при согласии пациента.
Меры, необходимые при пропуске одной или нескольких доз лекарственного препарата
Ревматоидный артрит и гигантоклеточный артериит
Если пациент пропустил введение еженедельной подкожной инъекции препарата Актемра® в течение 7 дней после запланированной даты, следующая доза вводится по графику. Если пациент пропустил введение подкожной инъекции препарата Актемра® при режиме дозирования 1 раз в 2 недели, и при этом с момента пропущенной дозы прошло менее 7 дней, пациент должен ввести пропущенную дозу препарата немедленно, а следующую дозу – согласно графику.
Системный ювенильный идиопатический артрит
Если пациент пропустил введение еженедельной подкожной инъекции препарата Актемра® в течение 7 дней после запланированной даты, следующая доза вводится по графику. Если пациент пропустил введение подкожной инъекции препарата Актемра® при режиме дозирования 1 раз в 2 недели, и при этом с момента пропущенной дозы прошло менее 7 дней, пациент должен ввести пропущенную дозу препарата немедленно, а следующую дозу – согласно графику.
Полиартикулярный ювенильный идиопатический артрит
Если пациент пропустил введение подкожной инъекции препарата Актемра® в течение 7 дней после запланированной даты, он должен ввести пропущенную дозу как можно скорее, а следующую дозу – согласно графику. Если пациент пропустил введение подкожной инъекции и с момента пропуска дозы прошло более 7 дней, либо пациент не уверен в дате следующей инъекции, ему следует связаться с врачом или фармацевтом.
Рекомендации по обращению за консультацией к медицинскому работнику для разъяснения способа применения лекарственного препарата
При наличии вопросов по применению препарата, обратитесь к лечащему врачу.
Доступные данные о передозировке препаратом Актемра® ограничены. Сообщалось об одном случае непреднамеренной передозировки препаратом в однократной дозе 40 мг/кг внутривенно у пациента с множественной миеломой. Нежелательных реакций не наблюдалось.
Не отмечалось также серьезных нежелательных реакций у здоровых добровольцев, которые получали препарат однократно в дозе до 28 мг/кг, однако наблюдалась нейтропения, требовавшая снижения дозы.
Для описания частоты нежелательных реакций используются следующие категории: очень часто (≥1/10), часто (от ≥1/100 до <1/10), нечасто (от ≥1/1000 до <1/100), редко (от ≥1/10000 до <1/1000) или очень редко (<1/10000).
Очень часто
− реакции в месте введения
− инфекции верхних дыхательных путей
− гиперхолестеринемия
Часто
− лейкопения, нейтропения, гипофибриногенемия
− конъюнктивит
− боль в животе, язвенный стоматит, гастрит
− периферический отек, реакции гиперчувствительности
− воспаление подкожной клетчатки, пневмония, инфекции ротовой полости, вызванные Herpes simplex, Herpes zoster
− повышение активности «печеночных» трансаминаз, увеличение массы тела, повышение уровня общего билирубина
− головная боль, головокружение
− кашель, одышка
− сыпь, зуд, крапивница
− артериальная гипертензия
Нечасто
− гипотиреоз
− стоматит, язва желудка
− дивертикулит
− гипертриглицеридемия
− нефролитиаз
Редко
− лекарственное поражение печени, гепатит, желтуха
− реакции анафилаксии (с летальным исходом)
− синдром Стивенса-Джонсона
Очень редко
− печеночная недостаточность
При возникновении нежелательных лекарственных реакций обращаться к медицинскому работнику, фармацевтическому работнику или напрямую в информационную базу данных по нежелательным реакциям (действиям) на лекарственные препараты, включая сообщения о неэффективности лекарственных препаратов
РГП на ПХВ «Национальный центр экспертизы лекарственных средств и медицинских изделий» Комитета медицинского и фармацевтического контроля Министерства здравоохранения Республики Казахстан
http://www.ndda.kz
Один шприц-тюбик содержит
активное вещество – тоцилизумаб, 162 мг,
вспомогательные вещества: полисорбат 80, L-аргинин гидрохлорид, L-метионин, L-гистидин, L-гистидина гидрохлорида моногидрат, вода для инъекций
Прозрачная или сильно опалесцирующая жидкость от бесцветного до желтоватого цвета.
По 0.9 мл раствора в одноразовые шприц-тюбики с корпусом из бесцветного стекла типа 1 (ЕФ), закрывающиеся с одной стороны поршнем, изготовленным из бутилкаучука, ламинированным фторполимером, и встроенной иглой для инъекций с другой стороны, закрытой колпачком из полиизопрена (со стороны иглы) и полипропилена.
Шприц-тюбик со встроенной иглой помещен в защитный корпус.
По 4 шприц-тюбика вместе с инструкцией по применению на казахском и русском языках помещают в пачку из картона.
3 года
Не применять по истечении срока годности.
Хранить в холодильнике (2°С – 8°С). Не замораживать. После извлечения из холодильника шприц-тюбик может храниться до 2 недель при температуре не выше 30°С.
Хранить шприц-тюбик(и) в картонной пачке для защиты от света и влаги.
Хранить в недоступном для детей месте!
По рецепту
Сведения о производителе
Веттер Фарма-Фертигунг ГмбХ и Ко. КГ, Германия
Schützenstrasse 87
88212 Равенсбург, Германия
Тел. + 49-751-3700-0
Факс + 49-751-3700-4000
info@vetter-pharma.com
Держатель регистрационного удостоверения
Ф. Хоффманн-Ля Рош Лтд., Швейцария
Grenzacherstrasse 124,
4070 Базель, Швейцария
Тел. + 41 61 688 11 11
Факс + 41 61 691 93 91
info@roche.com
Наименование, адрес и контактные данные (телефон, факс, электронная почта) организации на территории Республики Казахстан, принимающей претензии (предложения) по качеству лекарственных средств от потребителей и ответственной за пострегистрационное наблюдение за безопасностью лекарственного средства
ТОО «Рош Казахстан»
050051, Республика Казахстан,
г. Алматы, проспект Достык, д. 210
Тел. +7 (727) 321 24 24
kz.safety@roche.com, kz.quality@roche.com
Актемра®, шприц-тюбик
Важно внимательно прочитать, понять и следовать данным инструкциям, чтобы Вы или Ваш родитель/опекун правильно использовали шприц-тюбик препарата Актемра®. Данные инструкции не заменяют прохождения соответствующего обучения необходимой технике выполнения инъекций у Вашего лечащего врача. Ваш лечащий врач должен показать Вам, как правильно подготовиться к выполнению инъекции перед первой инъекцией с использованием шприц-тюбика препарата Актемра®. Задайте Вашему лечащему врачу любые интересующие Вас вопросы. Не пытайтесь выполнить инъекцию, пока не будете уверены, что понимаете как пользоваться шприц-тюбиком препарата Актемра®.
Пожалуйста, ознакомьтесь также с инструкцией по медицинскому применению препарата Актемра®, которая помещена в пачку со шприц-тюбиком, для получения подробной информации о препарате. При использовании препарата Актемра® важно оставаться под наблюдением Вашего лечащего врача.
Важная информация:
● Не используйте шприц, если он имеет признаки повреждения
● Не используйте, если препарат помутнел, изменил цвет или содержит видимые частицы
● Никогда не пытайтесь разобрать шприц
● Не снимайте колпачок с иглы до тех пор, пока не будете готовы выполнить инъекцию
● Не делайте инъекций через одежду
● Никогда не используйте шприц повторно
● Не прикасайтесь к спусковым клипсам, так как это может повредить шприц
Хранение
Храните шприц-тюбик препарата Актемра® и другие лекарственные препараты в недоступном для детей месте. Всегда храните шприц в холодильнике при температуре 2°C – 8°C. После извлечения из холодильника допускается хранение шприц-тюбика до 2 недель при температуре ниже 30°C. Шприц-тюбик должен всегда храниться в картонной упаковке. Не допускайте замораживания и защищайте препарат от воздействия света. Храните шприц в сухом месте.
Части шприц-тюбика
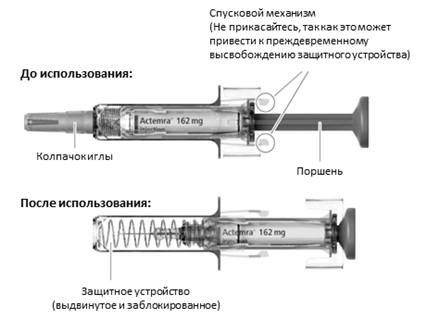
Для выполнения инъекции Вам понадобится следующее:
Включено в упаковку:
● Шприц-тюбик
Не включено в упаковку:
● Спиртовая салфетка
● Стерильный ватный тампон или марля
● Проколостойкий контейнер или контейнер для утилизации острых предметов для безопасной утилизации иглы и использованного шприца
Место для подготовки к инъекции:
● Найдите хорошо освещенную, чистую ровную поверхность, например, стол.
Шаг 1. Визуальный осмотр шприц-тюбика
● Извлеките упаковку со шприц-тюбиком из холодильника и откройте ее. Не прикасайтесь к спусковому механизму - это может повредить шприц-тюбик.
● Извлеките шприц-тюбик из упаковки и визуально осмотрите его и раствор в нем. Важно удостовериться, что шприц-тюбик и раствор безопасны для применения.
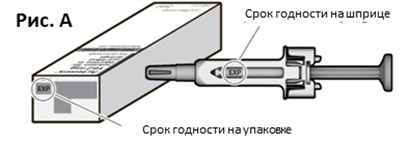
● Проверьте дату истечения срока годности на упаковке и шприц-тюбике (см. Рис. А), чтобы удостовериться, что срок годности не истек. Не используйте шприц-тюбик, если срок годности истек. Важно удостовериться, что шприц-тюбик и препарат безопасны для применения.
Шприц-тюбик нельзя использовать и следует его утилизировать, если:
● раствор помутнел
● раствор содержит посторонние видимые частицы
● раствор имеет цвет, отличный от бесцветного до светло-желтого
● любая часть шприц-тюбика имеет признаки повреждения.
Шаг 2. Согревание шприц-тюбика до комнатной температуры
● Не снимайте колпачок иглы со шприц-тюбика до Шага 5. Преждевременное снятие колпачка иглы может привести к высыханию препарата и блокированию просвета иглы.
● Поместите шприц-тюбик на чистую плоскую поверхность и оставьте его при комнатной температуре (18–28°C) приблизительно на 25–30 минут, для согревания. Если температура шприц-тюбика не достигла комнатной температуры, введение препарата может быть некомфортным, а ход поршня затрудненным.
● Не следует согревать шприц-тюбик любым другим способом.
Шаг 3. Обработка рук
● Вымойте руки водой с мылом.
Шаг 4. Выбор и подготовка места инъекции
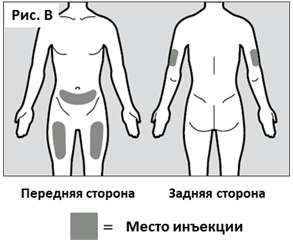
● Места, рекомендуемые для выполнения инъекции - передняя средняя часть бедра и нижняя часть живота (ниже пупка), за исключением области диаметром в пять сантиметров непосредственно вокруг пупка. (см. Рис. B).
● Если инъекцию выполняет родитель/опекун пациента, инъекцию можно также ввести в наружную поверхность плеча. (см. рис. В).
● Следует каждый раз менять место инъекции, как минимум на 3 сантиметра от места предыдущей инъекции.
● Не вводите препарат в участки, которые могут подвергаться раздражению ремнем или поясом одежды. Не вводите препарат в родинки, шрамы, синяки или места с нежной либо грубой кожей, покраснениями, уплотнениями или повреждениями.
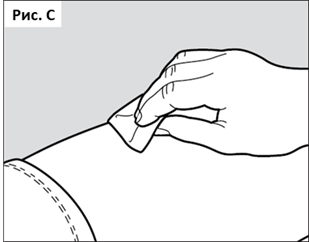
● Обработайте выбранное место инъекции, используя спиртовую салфетку (см. Рис С), для снижения риска инфицирования.
● Дайте коже высохнуть в течение примерно 10 секунд.
● Не прикасайтесь к обработанному участку до проведения инъекции. Не обдувайте и не обмахивайте обработанный участок.
Шаг 5. Снимите колпачок иглы
● Не держите шприц-тюбик за поршень при снятии колпачка иглы.
● Удерживая шприц-тюбик за защитный корпус одной рукой, осторожно снимите колпачок иглы другой рукой (см. Рис. D). Если Вы не можете снять колпачок иглы, обратитесь за помощью к родителю/опекуну или к медицинскому работнику.
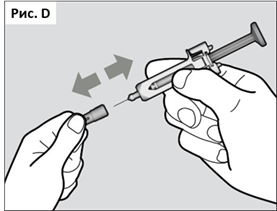
● Не прикасайтесь к игле и не позволяйте ей соприкасаться с любой поверхностью.
● Вы можете увидеть каплю жидкости на конце иглы. Это приемлемо.
● Поместите колпачок иглы в проколостойкий контейнер или контейнер для утилизации острых предметов.
ВНИМАНИЕ: После снятия колпачка иглы, шприц-тюбик следует использовать немедленно.
● Если шприц-тюбик не был использован в течение 5 минут после снятия колпачка иглы, он подлежит утилизации и помещению в проколостойкий контейнер или контейнер для утилизации предметов, и вместо него следует использовать новый шприц-тюбик. Если колпачок иглы был снят более чем на 5 минут, то выполнение инъекции может быть затруднено, поскольку лекарственный препарат может высохнуть и заблокировать просвет иглы.
● Никогда не надевайте колпачок иглы обратно на иглу после снятия.
Шаг 6. Введение препарата
● Удобно удерживайте шприц-тюбик одной рукой.
● Соберите пальцами свободной руки кожу в складку в месте инъекции, что быть удостовериться, что игла введена под кожу правильно. Это необходимо, чтобы препарат был введен под кожу (в жировую ткань), но не глубже (в мышцу). Введение иглы в мышцу может вызвать неприятные ощущения в месте введения.
● Не держитесь за поршень и не надавливайте на поршень, вставляя иглу в кожную складку.
● Полностью введите иглу в кожную складку под углом в диапазоне от 45° до 90° быстрым уверенным движением (см. Рис. Е).
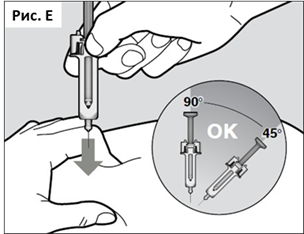
Важно выбрать правильный угол, чтобы обеспечить введение лекарственного препарата под кожу (в жировую ткань), в противном случае инъекция может быть болезненной, а лекарственный препарат может не подействовать.
● Удерживая шприц-тюбик в этом положении, отпустите кожную складку.
● Плавно нажимая на поршень до упора, медленно введите весь лекарственный препарат (см. Рис. F). Чтобы обеспечить введение полной дозы препарата, а также убедиться в том, что спусковой механизм находится в полностью выдвинутом положении, необходимо нажать поршень до упора. Если поршень нажат не до упора, то защитное устройство не выдвинется для закрытия иглы после ее извлечения. В случае если игла не закрыта, необходимо осторожно поместить шприц-тюбик в проколостойкий контейнер во избежание нанесения повреждений иглой.
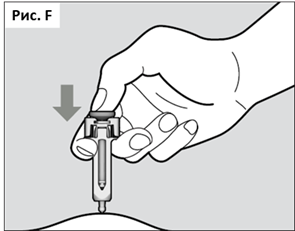
● После нажатия на поршень до упора перед извлечением иглы из кожи, не отпускайте поршень шприц-тюбика, чтобы убедиться, что лекарственный препарат введен полностью.
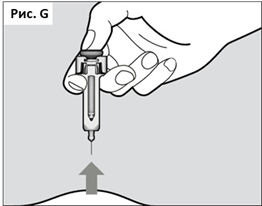
● Продолжая давить на поршень, извлеките иглу из кожи под тем же углом, под которым она была введена (см. Рис. G).
● Если после введения иглы Вы не можете сдвинуть поршень, то необходимо утилизировать шприц-тюбик в проколостойкий контейнер и использовать новый шприц-тюбик (начиная с Шага 2). Если трудности с подвижностью поршня сохраняются, то Вам следует проконсультироваться с Вашим лечащим врачом.
● После полного извлечения иглы из кожи Вы можете ослабить давление на поршень, тем самым позволяя защитному устройству закрыть иглу (см. Рис. H)
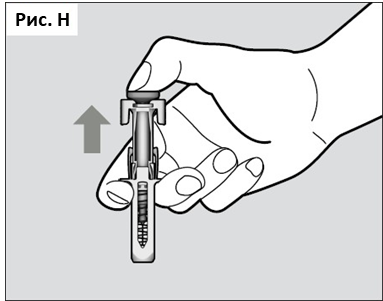
● При появлении крови в месте инъекции прижмите стерильный ватный тампон или марлевую салфетку к месту введения лекарственного препарата приблизительно на 10 секунд.
● Не растирайте место инъекции.
Шаг 7. Утилизация шприц-тюбика
● Не пытайтесь надеть колпачок иглы снова на шприц.
● Поместите использованные шприц-тюбики в проколостойкий контейнер или контейнер для утилизации острых предметов. Для получения информации о том, где приобрести «контейнер для утилизации острых предметов» или какие другие типы проколостойких контейнеров Вы можете использовать для безопасной утилизации использованных шприцев, обратитесь к Вашему лечащему врачу или фармацевту. (см. Рис. I)
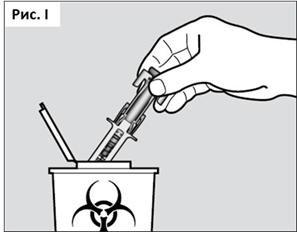
Обратитесь к своему лечащему врачу за инструкциями о надлежащей утилизации использованных шприцев в соответствии с местными требованиями.
Не выбрасывайте использованные шприцы или проколостойкий контейнер вместе с бытовыми отходами и не подвергайте их переработке.
● Утилизируйте заполненный контейнер в соответствии с указаниями врача или фармацевта.
● Всегда храните проколостойкий контейнер в недоступном для детей месте.
Инструкция для пациентов относительно реакции гиперчувствительности (также известной как реакция анафилаксии, если она выражена в тяжелой форме)
Если у Вас развиваются такие симптомы, как кожная сыпь, зуд, озноб, отек лица, губ, языка или горла, боль в груди, хрипы, затрудненное дыхание или глотание, головокружение или обморок во время или после инъекции препарата Актемра® в любое время когда Вы находитесь вне условий стационара, Вам следует немедленно обратиться за экстренной медицинской помощью.
Инструкция для раннего выявления и предотвращения риска развития серьезной инфекции
Будьте внимательны при проявлении первых признаков инфекции, таких как:
● боль в теле, лихорадка, озноб
● кашель, дискомфорт/стеснение в груди, одышка
● покраснение, жар, необычный отек кожи или сустава
● боль в животе/болезненная чувствительность и/или изменение функции кишечника
Позвоните своему лечащему врачу и немедленно обратитесь за медицинской помощью, если Вы подозреваете у себя симптомы развития инфекции.
Если у Вас есть какие-либо сомнения или вопросы по поводу использования шприц-тюбика, обратитесь за помощью к своему лечащему врачу или фармацевту.
| Актемра Раствор для подкожного введения шприцы преднаполненные 162 мг 0.9 мл ×4 | 79 900 тг. |