
Аджови, раствор, 225 мг 1.5 мл ×1
для подкожного введения шприцы, Тева ФП, Израиль • По рецепту
Шымкент
Каталог
Действующее вещество: Фреманезумаб

для подкожного введения шприцы, Тева ФП, Израиль • По рецепту

для подкожного введения шприцы, Веттер Фарма-Фертигун, Германия • По рецепту
Нервная система. Анальгетики. Антимигренозные препараты. Кальцитонин ген-родственного пептида антагонисты (Calcitonin gene-related peptide antagonists - CGRP). Фреманезумаб.
Код АТХ: N02CD03
Для профилактики мигрени у взрослых, имеющих по меньшей мере 4 дня с мигренью в месяц.
- повышенная чувствительность к действующему веществу, а также вспомогательным веществам, входящим в состав препарата
Предварительно заполненный шприц предназначен только для одноразового применения.
Не рекомендуется использовать Аджови если при визуальном осмотре раствор в шприце мутный, изменил цвет или содержит дополнительные частицы.
Не рекомендуется использовать Аджови, если раствор был прежде заморожен (например, в морозильной камере).
Не рекомендуется взбалтывать предварительно заполненный шприц.
ЗАПРЕЩАЕТСЯ использовать препарат, подвергнутый воздействию высоких температур или прямого солнечного света.
Прослеживаемость
Для улучшения прослеживаемости биологического лекарственного средства необходимо записать название и номер партии вводимого средства.
Необходимо немедленно обратиться к своему врачу, фармацевту или медсестре, при появлении каких-либо признаков серьезной аллергической реакции, например, затрудненного дыхания, отека губ и языка или сильной сыпи после инъекции Аджови. Эти реакции могут возникнуть в течение 24 часов после применения Аджови, но иногда могут быть отсрочены.
Вспомогательные вещества
В этом лекарственном средстве содержится менее 1 ммоль натрия (23 мг) на дозу, таким образом, оно является практически «безнатриевым». Один предварительно заполненный шприц содержит в качестве стабилизатора 99 мг сахарозы.
Официальных клинических исследований по лекарственному взаимодействию Аджови с другими средствами не проводилось. На основании характеристик фреманезумаба не ожидается фармакокинетических лекарственных взаимодействий. Кроме того, во время клинических исследований, одновременное применение лекарственных средств (в частности анальгетиков, спорыньи и триптанов) для лечения приступа мигрени и для профилактики мигрени, не повлияло на фармакокинетику фреманезумаба.
Пожилые пациенты (старше 65 лет)
В клинические исследования лекарственного препарата Аджови не было включено достаточное число пациентов в возрасте от 65 лет и старше для определения возможных отличий ответной реакции при введении препарата пациентам в возрасте 65 лет и старше от ответной реакции пациентов более молодого возраста.
Применение в педиатрии
Препарат не рекомендован к применению у пациентов до 18 лет, поскольку безопасность и эффективность препарата Аджови в данной возрастной группе не установлены.
Беременность
Имеются ограниченные данные по применению Аджови у беременных женщин. Исследования на животных не указывают на прямое или косвенное отрицательное воздействие в отношении токсического действия на репродуктивную систему. В качестве меры предосторожности рекомендуется избегать приема Аджови во время беременности.
Кормление грудью
Неизвестно, способен ли фреманезумаб проникать в грудное молоко. Установлено, что человеческий иммуноглобулин G (IgG) проникает в грудное молоко в течение первых дней после рождения и вскоре снижается до низких концентраций. Поэтому нельзя исключить риск для детей, находящихся на грудном вскармливании в течение этого короткого периода. Впоследствии использование фреманезумаба во время кормления грудью может быть рассмотрено только в случае клинической необходимости.
Препарат Аджови не влияет на способность управления транспортными средствами или работу с механизмами.
Режим дозирования
Лечение должно быть назначено врачом, имеющим опыт диагностики и лечения мигрени.
Существует две схемы терапии:
- 225 мг один раз в месяц (ежемесячно)
- 675 мг каждые три месяца (ежеквартально)
При переходе с одной схемы терапии на другую, новую дозу лекарственного препарата назначают в следующий запланированный день, согласно предыдущей схеме терапии.
На основании результатов анализа фармакокинетики фреманезумаба у пациентов 65 лет и старше корректировка дозы не требуется.
У пациентов с легкой или умеренной почечной или печеночной недостаточностью корректировка дозы не требуется.
Метод и путь введения
Препарат вводится только подкожно. Препарат не предназначен для внутривенного или внутримышечного введения. Шприц для инъекций, в котором содержится раствор препарата, предназначен только для одноразового использования.
Инъекция препарата Аджови проводится медицинским персоналом, пациентами и/или ухаживающими за ними лицами, обученными медицинским персоналом.
1. Убедитесь в том, что у Вас есть всё необходимое для инъекции: 1 (при дозе 225 мг) или 3 (при дозе 675 мг) одноразовых предварительно заполненных шприца с препаратом, салфетка, смоченная спиртом, ватный тампон, контейнер для использованных шприцев.
2. Вытащите упаковку из холодильника. Выдержите шприц с раствором при комнатной температуре не менее 30 минут. Не нагревайте одноразовый шприц, заполненный раствором препарата Аджови, горячей водой, в микроволновой печи или каким-либо другим способом, за исключением указанного, так как это может привести к непригодности раствора лекарственного средства.
3. Перед инъекцией извлеките одноразовый шприц, заполненный раствором препарата Аджови, из ячейкового контейнера, находящегося внутри картонной пачки. Не следует встряхивать шприц, заполненный раствором препарата, так как это может повлиять на работу медицинского устройства. Возможно, Вам понадобится более одного шприца, заполненного раствором препарата, согласно предписанной лечащим врачом дозе препарата Аджови.
4. Перед введением препарата Аджови тщательно вымойте руки с мылом.
5. Внимательно осмотрите раствор в шприце. Убедитесь, что раствор лекарственного препарата в шприце прозрачный от бесцветного до светло-желтого цвета. При наличии взвешенных частиц, комков, хлопьев или помутнений, изменений цвета, обесцвечивании или замораживании раствора его не следует применять. В растворе лекарственного препарата могут наблюдаться небольшие пузырьки воздуха. Не пытайтесь удалить воздушные пузырьки из предварительно заполненного шприца перед введением. Не используйте шприц, заполненный раствором препарата, если на поверхности шприца обнаруживаются видимые повреждения, например трещины или следы утечки препарата.
6. Выберите зону для инъекции. Возможные зоны для самостоятельных инъекций обозначены на рис.1: зона живота (отступив примерно на 5 см от пупка), передняя часть бедер (область, которая находится, по крайней мере, на 5 см выше колена и на 5 см ниже паха), задняя часть плеча. Для инъекций в труднодоступные зоны (например, задняя часть плеча) Вам может потребоваться помощь другого человека.
Не следует проводить инъекции в болезненные места, покрасневшие участки кожи, в области с огрубевшей кожей, с уплотнениями, гематомами, татуировками, шрамами или растяжками. Не следует вводить препарат Аджови в то же самое место, в которое был введен другой лекарственный препарат.
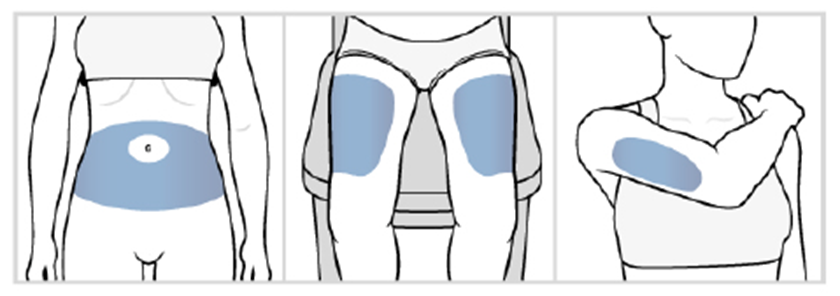
Рис.1 Схема расположения мест инъекций
Если при введении дозы препарата 675 мг Вы хотите использовать одну и ту же зону для трех отдельных инъекций (3 отдельных одноразовых предварительно заполненных шприца), убедитесь, что вторая и третья инъекции производятся не в то же место введения, которое Вы использовали для предыдущих инъекций.
7. Обработайте зону инъекции салфеткой, смоченной спиртовым раствором. Дайте высохнуть зоне инъекции в течение 10 секунд.
8. Снимите защитный колпачок с иглы. Не прокручивайте защитный колпачок. После снятия колпачка с иглы одноразового шприца не прикасайтесь к игле и не надевайте повторно защитный колпачок на иглу во избежание травмы или инфекции. Выбросьте защитный колпачок.
| 9. Предварительно слегка соберите не менее 2,5 см кожи в обработанной зоне для инъекции в складку большим и указательным пальцами (рис.2). |
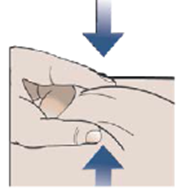 рис.2 |
| 10. Располагая иглу шприца под углом 45 – 90 градусов к месту инъекции, проколите кожу (рис.3). |
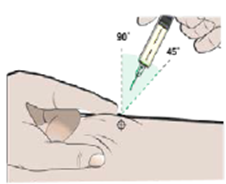 рис.3 |
| 11. Когда игла полностью войдет в кожу, равномерно надавливайте большим пальцем на поршень шприца (рис.4). |
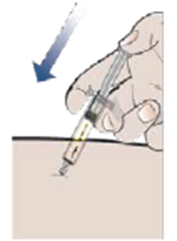 рис.4 |
| 12. Продолжайте медленное и равномерное надавливание на поршень, вводя содержимое шприца в место инъекции полностью (рис.5). |
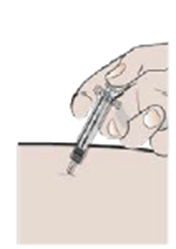 рис.5 |
| 13. Удалите шприц перпендикулярно месту инъекции (рис.6). |
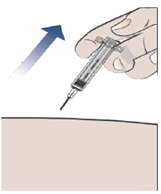 рис.6 |
14. Осторожно прижмите чистый ватный тампон к месту инъекции на несколько секунд.
15. Поместите шприц в контейнер для использованных шприцев и утилизируйте его.
Частота применения с указанием времени приема
При режиме введения препарата 225 мг (1 шприц) 1 раз в месяц, необходимо запланировать прием следующей дозы препарата через один месяц после последней введенной дозы. В случае режима введения препарата 675 мг (3 шприца) 1 раз в три месяца, необходимо запланировать прием следующей дозы препарата через три месяца после последней введенной дозы. Если у Вас появились вопросы по поводу графика введения, проконсультируйтесь с Вашим лечащим врачом.
Длительность лечения
При назначении лечения фреманезумабом сопутствующее профилактическое лечение мигрени может быть продолжено, если назначающий лечение врач посчитает это необходимым. Успешность лечения необходимо оценить в течение 3 месяцев после начала лечения.
В дальнейшем рекомендуется регулярно проводить оценку необходимости продолжения лечения. В каждом конкретном случае решение по продолжению лечения принимается индивидуально с учетом особенностей пациента.
Меры, необходимые при пропуске одной или нескольких доз лекарственного препарата
Если инъекция фреманезумаба пропущена в запланированную дату, ее следует ввести как можно скорее с учетом назначенной дозы и схемы применения.
Запрещено вводить двойную дозу с целью восполнения пропущенной дозы.
Обратитесь к врачу или фармацевту за советом прежде, чем принимать лекарственный препарат.
Дозы до 2000 мг вводились внутривенно в ходе клинических испытаний без дозоограничивающей токсичности. В случае передозировки рекомендуется убедиться, что у пациента отсутствуют признаки и симптомы нежелательных явлений, и в случае необходимости провести соответствующее симптоматическое лечение.
Очень часто
- болезненность в месте инъекции;
- уплотнения в месте инъекции;
- покраснение кожи в месте инъекции
Часто
- зуд в месте инъекции
Нечасто
- сыпь в месте инъекции
- крапивница, отек
Редко
- иммуногенность
- анафилактический шок
- серьезные аллергические реакции
Среди наиболее частых наблюдаемых местных реакций были болезненность, уплотнение и эритема в месте инъекции. Все местные реакции в месте инъекции были временными, преимущественно легкой или средней степени тяжести. Болезненность, уплотнение и эритема обычно наблюдались сразу же после инъекции, в то время как зуд и сыпь появлялись в среднем в течение 24 и 48 часов соответственно. Все реакции в месте инъекции проходили в основном в течение нескольких часов или дней. Реакции в месте инъекции обычно не требовали прекращения применения лекарственного средства.
Серьезные реакции гиперчувствительности
Анафилактические реакции сообщались в редких случаях. В основном реакции возникали в течение 24 часов после введения препарата, хотя в некоторых случаях наблюдались отсроченные реакции.
Иммуногенность
В плацебо-контролируемых исследованиях у 0,4% пациентов (6 из 1701), которые прошли курс лечения фреманезумабом, начали вырабатываться антитела к лекарственному препарату (ADA). Выработка антител была с низким титром. У одного из 6 пациентов начали вырабатываться нейтрализующие антитела. При продолжительности лечения 12 месяцев, антитела к лекарственному препарату были обнаружены у 2,3 % пациентов (43 из 1 888) и у 0,95% пациентов выработались нейтрализующие антитела. Выработка ADA не повлияла на безопасность и эффективность фреманезумаба.
При возникновении нежелательных реакций обращаться к медицинскому работнику, фармацевтическому работнику или напрямую в информационную базу данных по нежелательным реакциям (действиям) на лекарственные препараты, включая сообщения о неэффективности лекарственных препаратов
РГП на ПХВ «Национальный центр экспертизы лекарственных средств и медицинских изделий» Комитета медицинского и фармацевтического контроля Министерства здравоохранения Республики Казахстан
http://www.ndda.kz
Один мл препарата содержит
активное вещество – фреманезумаб, 150 мг (225 мг фреманезумаба в одном шприце);
вспомогательные вещества – L-гистидин, L-гистидина гидрохлорид моногидрат, сахароза, динатрия эдетата дигидрат, полисорбат 80, вода для инъекций.
Прозрачный или слегка опалесцирующий раствор от бесцветного до светло-желтого цвета.
По 1,5 мл препарата (225 мг фреманезумаба) помещают в стеклянный шприц типа I с уплотнителем поршня из бромбутилкаучука и с фиксированной иглой из нержавеющей стали, защищенной двойным колпачком.
По 1 или 3 предварительно заполненных шприцев вместе с инструкцией по применению на казахском и русском языках, помещают в картонную пачку с контролем первого вскрытия.
3 года.
Не применять по истечении срока годности!
Хранить в оригинальной упаковке при температуре от 2°C до 8°C.
Не замораживать!
Предварительно заполненный шприц следует хранить в картонной упаковке для защиты от света.
Допускается хранение до 7 дней при температуре до 30°C.
В случае хранения препарата вне холодильника более 7 дней, его необходимо утилизировать. После хранения при комнатной температуре не помещайте обратно в холодильник.
Хранить в недоступном для детей месте!
Отпускается по рецепту
Сведения о производителе
Vetter Pharma-Fertigung GmbH & Co. KG,
Mooswiesen 2, 88214, Равенсбург , Германия
тел.: 4975137000
факс: 972-2-6551781
Е-mail: info@vetter-pharma.com.
Сведения об упаковщиках
1.Vetter Pharma-Fertigung GmbH & Co. KG,
Mooswiesen 2, 88214 , Равенсбург , Германия
2. Merckle GmbH
Ludwig-Merckle-Strasse 389143, Блубойрен, Германия
Держатель регистрационного удостоверения
Teva Pharmaceutical Industries Ltd,
124 Dvora HaNevia St., 6944020, Тель-Авив, Израиль
Тел: 972-3-9267267
info@tevapharm.com
Наименование, адрес и контактные данные (телефон, факс, электронная почта) организации на территории Республики Казахстан, принимающей претензии (предложения) по качеству лекарственных средств от потребителей и ответственной за пострегистрационное наблюдение за безопасностью лекарственного средства
ТОО «ратиофарм Казахстан»,
050059 (А15Е2Р), г. Алматы, пр. Аль-Фараби 17/1,
БЦ «Нурлы-Тау», 5Б, 6 этаж.
Телефон: (727)3251615;
е-mail: info.tevakz@tevapharm.com;
веб сайт: www.kaz.teva
| Аджови Раствор для подкожного введения шприцы 225 мг 1.5 мл ×1 | от 121 560 тг. |
| Аджови Раствор для подкожного введения шприцы 225 мг 1.5 мл ×3 | 121 560 тг. |